下列各组元素原子核外电子排布符合半充满规则的是()A、MgB、CrC、SiD、Co
题目
下列各组元素原子核外电子排布符合半充满规则的是()
- A、Mg
- B、Cr
- C、Si
- D、Co
相似考题
参考答案和解析
更多“下列各组元素原子核外电子排布符合半充满规则的是()A、MgB、CrC、SiD、Co”相关问题
-
第1题:
某原子失去2个核外电子后的核外电子排布与Ar原子相同。该原子的元素符号为(),原子序数为()。参考答案: Ca;20。
-
第2题:
某元素原子的核外电子排布为1S22S22P63S1,该元素的原子序数为l1,核内质子数为11 ,元素符号为( )
正确答案:Na
-
第3题:
用元素符号填空:(均以天然存在为准)原子半径最大的元素是(), 第一电离能最大的元素是(),原子中3d半充满的元素是(),原子中4p半充满的元素是(),电负性差最大的两个元素是(), 化学性质最不活泼的元素是()。
正确答案:Fr;He;Cr和Mn;As;Cs和F;He -
第4题:
简述电子在原子核外排布的规则,并写出N、Cu的核外电子排布式。
正确答案: (1)能量最低-多电子原子在基态时,核外电子总是尽可能分布到能量最低的轨道,这称为能量最低原理。
(2)保里不相容原理-在同一个原子中没有四个量子数完全对应相同的电子。
(3)洪特规则-电子分布到能量相同的等价轨道时,总是尽量先以自旋相同的方向单独占据能量相同的轨道。
洪特规则的特例-由光谱实验结果得到,等价轨道全充满、半充满或全空的状态是比较稳定的。 -
第5题:
下列各组元素不符合对角线规则的是()
- A、Li和Mg
- B、Be和Al
- C、B和Si
- D、Co和Ni
正确答案:D -
第6题:
元素的性质随着元素原子序数的递增而周期性变化,是由于()引起的。
- A、原子量的递增
- B、原子的核外电子的递增
- C、原子的核外电子排布的周期性变化
- D、原子的质子数发生周期性变化
正确答案:C -
第7题:
元素单质的化学性质主要取决于()。
- A、原子核中的质子数
- B、原子核中的中子数
- C、原子质量数
- D、核外电子数及排布情况
正确答案:D -
第8题:
已知某副族元素A的原子,电子最后排入3d,最高氧化数为+4;元素B的原子,电子最后排入4p,最高氧化数为+5。回答下列问题: ⑴写出A、B元素原子的核外电子排布式。 ⑵根据核外电子排布式,指出它们在周期表中的位置(周期、族)。
正确答案:⑴A:1s22s22p63s23p63d24s2;B:1s22s22p63s23p63d104s24p3。
⑵A:第四周期ⅣB族;B:第四周期ⅤA族。 -
第9题:
第一电离能最大的元素是();电负性最大的元素是();原子中3d轨道半充满的元素是();原子中4p轨道半充满的元素是()。
正确答案:F;F;Cr Mn;As -
第10题:
简述原子核外电子排布三原则。
正确答案: 泡利不相容原理、最低能量原理、洪德规则 -
第11题:
具有全充满,半充满,全空三种状态的电子排布,属于核外电子排布的什么原则?()
- A、泡利不相容原理
- B、洪特规则
- C、空间性原则
- D、能量最低原理
正确答案:B -
第12题:
单选题具有全充满,半充满,全空三种状态的电子排布,属于核外电子排布的什么原则?()A泡利不相容原理
B洪特规则
C空间性原则
D能量最低原理
正确答案: A解析: 暂无解析 -
第13题:
某元素原子的核外电子排布为1S22S22P63S1,该元素的原子序数为(),核内质子数为(),元素符号为()。参考答案: ll;l1;Na
-
第14题:
下列各种表述中,两个微粒属于同种元素的原子的是( )。
A.3D能级有一个空轨道的基态原子和核外电子排布为1s22s22p63s23p2的原子
B.2p能级有一个未成对电子的基态原子和价电子排布为2s22p5的原子
C.M层全充满而N层4s2的原子和核外电子排布为1s22s22p63s23p63d24s2的原子
D.最外层电子数是核外电子总数的1/5的原子和价电子排布为4s24p3的原子答案:A解析:A项,3p能级有一个空轨道的基态原子的核外电子排布为1s22s22p63s23p2,A项描述的是同种元素的原子;B项,2p能级有一个未成对电子的基态原子的核外价电子排布有两种情况:2s22p1、2s22p5,B项描述的不一定是同种元素的原子:C项.M层全充满而N层为4s:的原子的核外电子排布为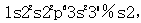 ,c项描述的不是同种元素的原子;D项.最外层电子数是核外电子总数的1/5的原子是Br,其核外电子排布为 )
,c项描述的不是同种元素的原子;D项.最外层电子数是核外电子总数的1/5的原子是Br,其核外电子排布为 )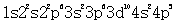 .D项描述的不是同一种元素的原子;故本题选A。
.D项描述的不是同一种元素的原子;故本题选A。 -
第15题:
元素的性质主要决定于核外电子的排布,特别是()的排布。
正确答案:最外层电子 -
第16题:
原子核外电子排布的原则是()。
- A、能力最低原理
- B、泡利不相容原理
- C、洪特规则
- D、以上均是
正确答案:D -
第17题:
通过元素周期表,可以知道元素的()。
- A、符号
- B、原子量
- C、电子数
- D、核外电子排布
正确答案:A,B,C -
第18题:
元素的性质随着原子序数的递增呈现周期性变化的原因是()。
- A、元素原子的核外电子排布呈周期性变化
- B、元素原子的电子层数呈现周期性变化
- C、元素化合价呈周期性变化
- D、元素原子半径呈周期性变化
正确答案:A -
第19题:
原子中4p半充满的元素是(),3d半充满的元素是()。
正确答案:As;Cr和Mn -
第20题:
原子序数为17的元素,其原子核外电子排布式为();未成对电子数为1。
正确答案:1s22s22p63s23p5 -
第21题:
写出下列元素原子或离子的核外电子排布式: (1)Cr3+:()。 (2)P:() (3)Ca2+:()。 (4)Ni:()。
正确答案: 1S22S22P63S23P64d3;1S22S22P63S23P3;1S22S22P63S23P6;1S22S22P63S23P64d84S2 -
第22题:
若把某元素原子核外电子排布写成(n-1)d4ns2时,违背了()
- A、保里不相容原理
- B、能量最低原理
- C、洪特规则
- D、洪特规则特例
正确答案:D -
第23题:
问答题简述电子在原子核外排布的规则,并写出N、Cu的核外电子排布式。正确答案: (1)能量最低-多电子原子在基态时,核外电子总是尽可能分布到能量最低的轨道,这称为能量最低原理。
(2)保里不相容原理-在同一个原子中没有四个量子数完全对应相同的电子。
(3)洪特规则-电子分布到能量相同的等价轨道时,总是尽量先以自旋相同的方向单独占据能量相同的轨道。
洪特规则的特例-由光谱实验结果得到,等价轨道全充满、半充满或全空的状态是比较稳定的。解析: 暂无解析
