向0.4L2.5mol/L的NaNO3溶液中加入()5mol/LNaNO3溶液可使其摩尔浓度达到4.5mol/L。A、2LB、2.4LC、3LD、1.6L
题目
向0.4L2.5mol/L的NaNO3溶液中加入()5mol/LNaNO3溶液可使其摩尔浓度达到4.5mol/L。
- A、2L
- B、2.4L
- C、3L
- D、1.6L
相似考题
参考答案和解析
更多“向0.4L2.5mol/L的NaNO3溶液中加入()5mol/L”相关问题
-
第1题:
室温下,向l0mLpH=3的醋酸溶液中加入水稀释后,下列说法正确的是()。
A.溶液中醋酸的电离平衡常数不变
B.溶液中导电粒子的数目增多,导电性增强
C.醋酸的电离程度增大,pH减小
D.再加入l0mLpH=11的NaOH溶液,混合溶液pH=7答案:A解析:温度不变,电离平衡常数不变。因醋酸溶液加水稀释,促进电离,则溶液中导电粒子的数目增多.但是稀释过后,离子浓度变小。导电性变差。醋酸属于弱酸,加水稀释,电离程度变大,但是溶液的体积增大的倍数大于n(H+)增加的倍数,则C(H+)减小,pH增大。等体积pH=3的醋酸与pH=11的NaOH溶液混合时,醋酸的浓度大于0.001 mol/L,醋酸过量,则溶液的pH<7。故本题选A。 -
第2题:
强心苷强烈酸水解的条件是A.3~5mol/L盐酸长时间加热
B.3~5mol/L盐酸长时间加热加压
C.3~5mol/L盐酸短时间加热加压
D.3~5moI/L盐酸短时间加热
E.3~5mol/L盐酸时间加压答案:B解析:强心苷强烈酸水解的条件是3~5mol/L盐酸长时间加热加压,所以答案为B。 -
第3题:
欲配制1升浓度为1mcl/L硫酸溶液应取5mol/L的标准硫酸溶液多少毫升?
正确答案: 设5mol/L的标准硫酸溶液为毫升,则有:5=1×1000
∴=1000/5=200(ml) -
第4题:
5mol/l烧碱溶液能稀释成0.05M的溶液()ml
- A、95ml
- B、100ml
- C、105ml
正确答案:B -
第5题:
将20毫升1mol/L硫酸溶液加入到另外一20毫升1mol/L硫酸溶液中溶液中,则混合液的浓度是2mol/L。()
正确答案:错误 -
第6题:
向0.4L2.5mol/L的NaNO3溶液中加入()5mol/LNaNO3溶液可使其摩尔浓度达到4.5mol/L。
- A、2L
- B、2.4L
- C、3L
- D、1.6L
正确答案:D -
第7题:
向1L1mol/L的处于等电点的甘氨酸溶液加入0.3molHCl,问所得溶液的pH是多少,如果加入0.3mol NaOH以代替HCl时,pH将是多少?
正确答案: 解:
P.H1=pKa1+lg(7/3)=2.71
P.H2=pKa2+lg(3/7)=9.23 -
第8题:
强心苷强烈酸水解的条件是()
- A、3~5mol/L盐酸长时间加热
- B、3~5mol/L盐酸长时间加热加压
- C、3~5mol/L盐酸短时间加热加压
- D、3~5moI/L盐酸短时间加热
- E、3~5mol/L盐酸时间加压
正确答案:B -
第9题:
欲使CaCO3在水溶液中溶解度增大,可以采用的最好方法是()。
- A、加入1.0mol.L-1Na2CO3
- B、加入2.0 mol.L-1NaOH
- C、加入0.10mol.L-1EDTA
- D、降低溶液的pH值
正确答案:D -
第10题:
问答题向1L1mol/L的处于等电点的甘氨酸溶液加入0.3molHCl,问所得溶液的pH是多少,如果加入0.3mol NaOH以代替HCl时,pH将是多少?正确答案: 解:
P.H1=pKa1+lg(7/3)=2.71
P.H2=pKa2+lg(3/7)=9.23解析: 暂无解析 -
第11题:
单选题把80mLNaOH溶液加入到120mL盐酸中,所得溶液的pH值为2.如果混合前NaOH溶液和盐酸的物质的量浓度相同,它们的浓度是()A05mol/L
B01mol/L
C005mol/L
D1mol/L
正确答案: C解析: 暂无解析 -
第12题:
单选题强心苷强烈酸水解的条件是()A3~5mol/L盐酸长时间加热
B3~5mol/L盐酸长时间加热加压
C3~5mol/L盐酸短时间加热加压
D3~5moI/L盐酸短时间加热
E3~5mol/L盐酸时间加压
正确答案: D解析: 强心苷强烈酸水解的条件是3~5mol/L盐酸长时间加热加压,所以答案为B。 -
第13题:
在0.1 mol/L的CH3COOH溶液中存在如下电离平衡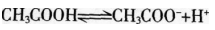 ,对该平衡下列叙述中,正确的是( )。
,对该平衡下列叙述中,正确的是( )。
A.加入水后,平衡向逆反应方向移动
B.加入0.1 mol/L的HCl溶液,溶液中c(H+)减小
C.加入少量NaOH固体,平衡向正反应方向移动
D.加入少量CH3COONa固体.平衡向正反应方向移动答案:C解析:加水稀释,平衡向右移动,A项错误;加入HCl溶液,引入了H+,平衡向左移动,但c(H+)增大,B项错误;加入少量NaOH固体,中和了部分H+,平衡向右移动,C项正确;加入CH3COONa,。(CH3COOH-)增大。平衡向左移动。D项错误。 -
第14题:
欲配V为5L、c为5mol/L的硫酸溶液,需用ρ=1.84g/cm3、纯度95%的H2SO4多少毫升?
正确答案:c1V1=c2V2
V1=c2V2/c1=5×5×98/(1.84×95%)=1402(mL)
需用纯度95%的H2SO41402mL。 -
第15题:
C(1/2H2SO4)=5mol/L,那么该1L溶液中含()gH2SO4。
- A、 1×49
- B、 5×49
- C、 96
- D、 5×98
正确答案:B -
第16题:
强心苷强烈酸水解的条件是()。
- A、3~5mol/L盐酸长时间加热
- B、3~5mol/L盐酸长时间加热加压
- C、3~5mol/L盐酸短时间加热加压
- D、3~5mol/L盐酸短时间加热
- E、3~5mol/L盐酸时间加压
正确答案:B -
第17题:
C(1/2H2SO4)=5mol/L,那么该溶液中基本单元的摩尔质量是()。
- A、 2
- B、 49
- C、 98
- D、 96
正确答案:B -
第18题:
向1.0L0.10mol·L-1HAc溶液中加入1.0mL0.010mol·L-1HCl溶液,下列叙述正确的是()。
- A、HAc解离度减小
- B、溶液的pH为3.02
- C、KaΘ(HAc)减小
- D、溶液的pH为2.30
正确答案:A -
第19题:
于0.1升0.10 mol.L-1的HAc溶液中加入0.01mol固体NaAc(假设体积不变)则溶液中的H+离子浓度将会();pH将会(),Ac-离子浓度将会()(填增大、减小或不变)。该混合溶液称为()溶液,其H+离子浓度为()mol.L-1,向该溶液中加入少量酸、碱或水后,溶液pH为()。
正确答案:减小;增大;增大;缓冲;1.76×10-5;不变 -
第20题:
向25mL0.1mol/LKI溶液中加入10mL0.005mol/LAgNO3溶液所制得的AgI溶胶的胶团结构为(),该溶胶的胶粒带()电荷。如果NaNO3对该溶胶的聚沉值为60mmol/L,Ca(NO3)2对该溶胶的聚沉值为()mmol/L。使溶胶稳定的三大因素是(),使溶胶聚沉的三种主要方法是()
正确答案:[(AgI)m·nI-·(n-x)K+]x-·xK+;负;30;布朗运动、电荷、水化膜;加电解质、加异电溶胶、高分子敏化 -
第21题:
问答题欲配5mol/L的H2SO4溶液5L,需用ρ=1.84g/cm3纯度95%的H2SO4多少毫升?正确答案: c1V1=c2V2
V1=5×5×98/(1.84×95%)=1402(mL)解析: 暂无解析 -
第22题:
单选题5mol/l烧碱溶液能稀释成0.05M的溶液()mlA95ml
B100ml
C105ml
正确答案: C解析: 暂无解析 -
第23题:
单选题向200mL0.1mol/L Na2SO4溶液中加入100mL0.25mol/L的Ba(OH)2溶液后,还需加入多少盐酸才能恰好完全中和( ).A10mL lmol/L盐酸
B5mL lmol/L盐酸
C50mL lmol/L盐酸
D25mL 0.5mol/L盐酸
正确答案: A解析:
Ba(OH)2溶液加入后对氢氧根离子没有消耗,所以溶液中的氢氧根离子的物质的量为为0.05mol,所以需要0.05mol的氢离子来中和. -
第24题:
问答题欲配制1升浓度为1mcl/L硫酸溶液应取5mol/L的标准硫酸溶液多少毫升?正确答案: 设5mol/L的标准硫酸溶液为毫升,则有:5=1×1000
∴=1000/5=200(ml)解析: 暂无解析
