为了从粗盐(其中含K+、Ca2+、Mg2+、SO42-及泥沙等杂质)中提纯得到氯化钠,可将粗盐溶于水后,进行一系列操作。请将这些操作简要地写在下面空白处。
题目
为了从粗盐(其中含K+、Ca2+、Mg2+、SO42-及泥沙等杂质)中提纯得到氯化钠,可将粗盐溶于水后,进行一系列操作。请将这些操作简要地写在下面空白处。
相似考题
更多“为了从粗盐(其中含K+、Ca2+、Mg2+、SO42-及泥沙等杂质)中提纯得到氯化钠,可将粗盐溶于水后,进行一系列操作。请将这些操作简要地写在下面空白处。”相关问题
-
第1题:
(3)粗盐提纯时蒸发滤液所用到的仪器是______________。
正确答案:
cdg -
第2题:
已知所含元素化合价发生变化的反应是氧化还原反应,其中被还原的元素化合价降低,被氧化的元素化合价升高。海洋中有丰富的资源,如下图所示利用海水可获得许多化工产品。下列有关说法正确的是 ( ) A.第①步中除去粗盐中的SO42-、Ca2+、Mg2+等杂质,加入的试剂顺序为:Na2CO3溶液、NaOH溶液、BaCl2溶液,过滤后加盐酸
A.第①步中除去粗盐中的SO42-、Ca2+、Mg2+等杂质,加入的试剂顺序为:Na2CO3溶液、NaOH溶液、BaCl2溶液,过滤后加盐酸
B.第②步中加入的试剂为CaCl2溶液
C.第③步中发生分解反应
D.在第④步中溴元素被还原答案:C解析: -
第3题:
地下水中含量较多,分布最广的几种离子是:
A. H+、Mg2+、OH-、HCO3-
B. K+、Na+、Ca2+、Mg2+、Cl-、SO42-、HCO3-
C. H+、OH-、CO2、Cl-、HCO3-
D. K+、Na+、Cl-、SO42-、HCO3-答案:B解析:提示:地下水中主要的离子成分有K+、Na+、Ca2+、Cl-、SO42-、HCO3-。 -
第4题:
小红同学在家做“粗盐提纯”的实验,下列对其做法的认识中,错误的是()
- A、将粗盐放入玻璃杯中加水溶解—粒子在不断运动
- B、溶解时用筷子搅拌——加快溶解速度
- C、用自制净水器过滤粗盐水——可将粗盐水变成纯净物
- D、实验时不用一次性塑料杯或纸杯——保护环境要从身边小事做起
正确答案:C -
第5题:
为了从粗盐(其中含K+、Ca2+、Mg2+、SO42-及泥沙等杂质)中提纯得到氯化钠,可将粗盐溶于水后,进行一系列操作。在提纯过程中,在加入相应试剂后,都会把溶液加热至微沸,并保持一段时间,为什么呢?
正确答案:增加离子碰撞机会使沉淀完全。 -
第6题:
欲将粗盐提纯并用所得精盐配制一定质量分数的氯化钠溶液。下列说法正确的是()
- A、粗盐过滤时,用玻璃棒搅拌加快过滤的速度
- B、蒸发滤液时,待蒸发皿中滤液蒸干时停止加热
- C、配制溶液需要经过计算、称量、溶解、装瓶贴标签等步骤
- D、配制溶液时必须使用的仪器有托盘天平、酒精灯、量筒、烧杯、玻璃棒等
正确答案:C -
第7题:
阳离子交换器中主要去除水中的阳离子如K+、Na+、Ca2+、Mg2+等可溶性杂质
正确答案:正确 -
第8题:
如何将粗食盐中常含有的杂质Ca2+ 、Mg2+ 和SO42-除去?
正确答案:加入适量BaCl2、Na2CO3和NaOH,分别生成BaSO4、CaCO3、Mg(OH)2 、BaCO3沉淀。 -
第9题:
用足量的含不溶性固体杂质(其含量不详)的粗盐,经提纯后配制成一定溶质质量分数的NaCl溶液,实验操作有:①称量; ②过滤; ③蒸发结晶; ④计算; ⑤溶解; ⑥干燥。 其先后顺序正确的是()
- A、④①⑤
- B、⑤②③⑥
- C、⑤②③⑥④①⑤
- D、④①⑤②③⑥⑤
正确答案:C -
第10题:
单选题用足量的含不溶性固体杂质(其含量不详)的粗盐,经提纯后配制成一定溶质质量分数的NaCl溶液,实验操作有:①称量; ②过滤; ③蒸发结晶; ④计算; ⑤溶解; ⑥干燥。 其先后顺序正确的是()A④①⑤
B⑤②③⑥
C⑤②③⑥④①⑤
D④①⑤②③⑥⑤
正确答案: C解析: 用粗盐配制溶液,应选除杂、干燥、计算、称量,再配制。 -
第11题:
单选题小红同学在家做“粗盐提纯”的实验,下列对其做法的认识中,错误的是()A将粗盐放入玻璃杯中加水溶解—粒子在不断运动
B溶解时用筷子搅拌——加快溶解速度
C用自制净水器过滤粗盐水——可将粗盐水变成纯净物
D实验时不用一次性塑料杯或纸杯——保护环境要从身边小事做起
正确答案: C解析: 暂无解析 -
第12题:
单选题由盐田中靠晒干海水所得到的是()。A可以直接出售
B粗盐
C精盐
D含碘盐
正确答案: A解析: 暂无解析 -
第13题:
为了除去粗盐中的Ca2+、Mg2+.S042-及泥涉可将粗盐溶于不然后进行下列五项操作:①过滤②加过量NaOH溶液③加适量盐酸④加过量Na2C03溶液⑤加过量BaCl2溶液。正确的操作顺序是( )。
A.①④②⑤③
B.④①②⑤③
C.②⑤④①③
D.⑤②④①③
正确答案:CD
-
第14题:
通过海水晾晒可得粗盐。粗盐除NaCl外,还含有MgCl2、CaCl2以及泥沙等杂质。为了有效将粗盐提纯,实验的各步操作流程如下图所示。
根据以上信息回答:
(1)在完成操作Ⅰ之前,必须加入的X物质是( ) 。
(2)操作Ⅰ和操作Ⅱ的名称是( )。该操作中需要将圆形滤纸折叠处理,下列图示中不该出现的情形是( ) (填序号)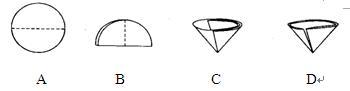
(3)在蒸发操作中容易造成食盐固体飞溅,为尽量减少飞溅,除连续搅拌外还可采取( )等措施。
(4)在实验过程中加入过量的NaOH溶液,其实验目的是( ) 。
(5)判断加入的盐酸“适量”的方法是( )。
(6)实验所得精盐的质量_________(填“大于”、“小于”或“等于”)粗盐中NaCl的质量,原因是( )。
答案:解析:(1)水
(2)过滤 D
(3)间歇加热(或“来回移动酒精灯或蒸发皿”)
(4)除尽溶液中的镁离子
(5)滴加盐酸至无气泡放出为止
(6)大于 提纯的过程中有氯化钠生成 -
第15题:
精制反应的粗盐水中的机械杂质一般采用澄清和过滤的方法除去。
正确答案:正确 -
第16题:
用于除去水中机械杂质、细菌、有机物、气体、阳离子、阴离子的过程(如Ca2+、Mg2+、Cl-、SO42-等)是水处理过程。
正确答案:正确 -
第17题:
含有Ca2+﹑Mg2+和SO42-离子的粗盐如何精制成纯的食盐,以反应式表示。
正确答案: (1)SO42-+Ba2+=BaSO4↓
(2)Mg2++2OH-=Mg(OH)2↓
(3)Ca2++CO32-=CaCO3↓
(4)Ba2++CO32-=BaCO3↓
(5)CO32-+2H+=CO2↑+H2O
OH-+H+=H2O -
第18题:
为了除去粗盐中的Ca2+、Mg2+.S042-及泥涉,可将粗盐溶于不,然后进行下列五项操作:①过滤,②加过量NaOH溶液,③加适量盐酸,④加过量Na2C03溶液,⑤加过量BaCl2溶液。正确的操作顺序是()。
- A、①④②⑤③
- B、④①②⑤③
- C、②⑤④①③
- D、⑤②④①③
正确答案:C,D -
第19题:
精盐是把粗盐溶解为水,除去杂质后再()而成。
正确答案:蒸发结晶 -
第20题:
粗盐提纯实验有几步操作?在各步操作中玻璃棒各起什么作用?
正确答案: 粗盐提纯的步骤是:①溶解;②过滤;③蒸发结晶.溶解时玻璃棒的作用是:搅拌,加速粗盐的溶解;过滤时玻璃棒的作用是:引流,使液体沿着玻璃棒流进过滤器,防止溅出.蒸发时玻璃棒的作用是:搅拌,使液体均匀受热,防止局部过热而溅出. -
第21题:
地层水的化学成分主要有()等阳离子和Cl-、SO42-、CO32-、CHO3-等阴离子。
- A、K+、Ca2+、Mg2+
- B、Na+、Ca2+、Mg2+
- C、Na+、K+、Mg2+
- D、Na+、K+、Ca2+、Mg2+
正确答案:D -
第22题:
单选题欲将粗盐提纯并用所得精盐配制一定质量分数的氯化钠溶液。下列说法正确的是()A粗盐过滤时,用玻璃棒搅拌加快过滤的速度
B蒸发滤液时,待蒸发皿中滤液蒸干时停止加热
C配制溶液需要经过计算、称量、溶解、装瓶贴标签等步骤
D配制溶液时必须使用的仪器有托盘天平、酒精灯、量筒、烧杯、玻璃棒等
正确答案: A解析: 暂无解析 -
第23题:
单选题“粗盐提纯”的实验中,蒸发时,正确的操作是( ).A把混浊的液体倒入蒸发皿内加热
B蒸发皿中出现大量固体时即停止加热
C开始析出晶体后用玻璃棒搅拌
D待水分完全蒸干后停止加热
正确答案: B解析:
A项,应该先将粗盐溶解过滤掉其中的杂质;B项,有大量固体析出的时候,就停止加热,余热能把余下的水分蒸干的,但是必须用玻璃棒不断搅动,以免固体飞溅;C项,晶体析出后就不需要再继续用玻璃棒搅拌了,只有在晶体还没有析出时才需要搅拌;D项,有大量固体析出的时候,就停止加热.
