测量一定质量的铝锌合金与强酸溶液反应产生氢气的体积,可以求得合金中铝和锌的质量分数.现有下列实验用品:中学实验常用仪器、800mL烧杯、100mL量筒、短颈玻璃漏斗、铜网、铝锌合金样品、浓盐酸(密度1.19g/cm3)、水. 补充下列实验步骤,直到反应开始进行(铁架台和铁夹的安装可省略). ①________________________________________________________________________ ②________________________________
题目
测量一定质量的铝锌合金与强酸溶液反应产生氢气的体积,可以求得合金中铝和锌的质量分数.现有下列实验用品:中学实验常用仪器、800mL烧杯、100mL量筒、短颈玻璃漏斗、铜网、铝锌合金样品、浓盐酸(密度1.19g/cm3)、水. 补充下列实验步骤,直到反应开始进行(铁架台和铁夹的安装可省略). ①________________________________________________________________________ ②________________________________________________________________________ ③________________________________________________________________________ ④________________________________________________________________________
相似考题
更多“测量一定质量的铝锌合金与强酸溶液反应产生氢气的体积,可以求得合金中铝和锌的质量分数.现有下列实验用品:中学实验常用仪器、800mL烧杯、100mL量筒、短颈玻璃漏斗、铜网、铝锌合金样品、浓盐酸(密度1.19g/cm3)、水. 补充下列实验步骤,直到反应开始进行(铁架台和铁夹的安装可省略). ①________________________________________________________________________ ②________________________________”相关问题
-
第1题:
铝与下列物质反应时不能放出氢气的是( )A.稀硫酸
B.浓硝酸
C.浓烧碱溶液
D.浓盐酸答案:B解析: -
第2题:
玻璃棒是化学实验中常用的仪器,其作用是用于搅拌、过滤或转移液体时引流等。下列有关实验过程中,肯定不需要使用玻璃棒进行操作的是( )。A.一定溶质物质的量浓度溶液的配制
B.硫酸铜晶体里结晶水含量测定的实验
C.用已知浓度的盐酸和未知浓度的氢氧化钠溶液进行中和滴定实验
D.用浓氨水和浓盐酸进行氨和氯化氢反应的实验答案:C解析:在中和滴定实验中不需要玻璃棒,其余都需要,答案选C。 -
第3题:
阅读下面文字.回答有关问题:
检验铝与盐酸、铝与氢氧化钠反应。通常的做法是在2支小试管里分别加入5 mL盐酸和5 mL NaOH溶液,再分别放一段铝片,观察实验现象,过一段时间后,将点燃的木条分别放在2支试管口。下面是某老师对铝与盐酸、铝与氢氧化钠反应实验的改进:
在2支小试管里分别加入5 mL盐酸和5 mL NaOH溶液,再各加入2滴CuS04溶液,再分别放一段铝片,观察实验现象,过一段时间后,将点燃的木条分别放在2支试管口。观察实验现象。
结合上述材料.简要回答问题:(1)简述教师为什么做上述改进。(2)简述中学化学实验改进的原则。(任意写出3点)答案:解析:由于铝表面有致密的氧化膜.改进之前的实验往往要等40分以后才能看到铝片上产生大量的气泡,很难完成40分钟的课堂教学任务。改进之后,Cu2+在铝表面被还原成铜单质 -
第4题:
2×××系列铝合金是()。
- A、含工业纯铝98%的金属
- B、铜为主要合金添加元素
- C、高强度铝锌合金
- D、主要合金添加元素是镁和铬
正确答案:B -
第5题:
锌合金是以锌为基体加入一定量的()等元素而形成,以提高高锌的强度、硬度和耐磨性
- A、铝、镁、碳
- B、铝、锰、碳
- C、铜、铝、锰
- D、铜、铝、镁
正确答案:A -
第6题:
在测量盐水密度的实验步骤中,下列步骤中不必要的是()
- A、用天平测出烧杯的质量m1
- B、往烧杯内倒入适量的盐水,用天平测出烧杯和盐水的总质量m1
- C、用量筒测出烧杯中液体的体积V
- D、用天平测出倒掉盐水后空烧杯的质量m2
正确答案:A -
第7题:
小明准备做过滤实验,老师给了他如下仪器:漏斗、烧杯、滤纸、铁架台。他认为还应补充一种仪器,这种仪器应是()。
- A、小烧杯
- B、玻璃棒
- C、药匙
- D、长颈漏斗
正确答案:B -
第8题:
锌铝合金和铝锌合金镀层的厚度可通过中性耐盐雾实验确定,其耐盐雾性能不应小于500小时。
正确答案:错误 -
第9题:
配制0.1mol∕L盐酸溶液1000mL,需用密度为ρ=1.19g∕cm3、质量分数为37.23﹪的浓盐酸()mL。
正确答案:8.23 -
第10题:
7075-T6铝合金是()。
- A、经过固溶热处理和人工时效的铝锌合金。
- B、经过固溶热处理和人工时效的铝铜合金。
- C、仅作人工时效处理的铝锌合金。
- D、仅作人工时效处理的铝铜合金。
正确答案:A -
第11题:
单选题在测量盐水密度的实验步骤中,下列步骤中不必要的是()A用天平测出烧杯的质量m1
B往烧杯内倒入适量的盐水,用天平测出烧杯和盐水的总质量m1
C用量筒测出烧杯中液体的体积V
D用天平测出倒掉盐水后空烧杯的质量m2
正确答案: B解析: 暂无解析 -
第12题:
填空题碱溶法一般以质量分数为20%——30%的()溶液作溶剂,主要用于分解金属铝及铝、锌等有色合金。反应应在()或()烧杯中进行。正确答案: 氢氧化钠,银烧杯,聚四氟乙烯解析: 暂无解析 -
第13题:
下面是铝热反应的改进实验。
(1)实验用品:2g氧化铁和铝粉的混合物(质量比5:2)、氯酸钾、无水乙醇、粉笔l支、烧杯、镊子、药匙、玻璃片、带铁夹的铁架台、盛细沙的蒸发皿、磁铁、火柴、小刀。
(2)实验步骤?
①用小刀在干粉笔上挖出宽约0.5?cm、深约0.3?cm的浅槽后.将粉笔浸泡于盛有无水乙醇的烧杯中。
②用镊子取出浸透乙醇的粉笔于玻璃片上.用药匙把2g混合好的铝热剂平铺在粉笔槽中,上面再铺少许氯酸钾。
③将盛药品的粉笔倾斜固定在铁夹上,并在下方放置盛细沙的蒸发皿。
④用火柴点燃粉笔,观察实验现象。
根据上述材料,简要回答下列问题:?
(1)该实验可以观察到的现象有哪些?写出发生反应的化学方程式。
(2)该改进实验在教学中有哪些优点?答案:解析:(1)氧化铁粉末和铝粉发生剧烈反应,放出大量的热,发出耀眼的光芒;熔融物落入细沙中,待冷却后,可用磁铁吸引。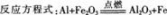
(2)该改进实验的优点:
①药品用量减少,提高了演示实验的安全性,演示时不会对前排学生构成事故威胁。
②由于没有使用镁条和滤纸折成的漏斗,所以没有镁条燃烧的强光和滤纸烧糊这些无关现象的干扰,便于学生观察和记忆。 -
第14题:
小黄用右图装置测定铜锌合金中锌的质量分数和锌的相对原子质量。主要实验步骤如下(必要的固定装置已略去):
①连接装置并检查装置气密性;
②加入药品和水;
③记录C中液面刻度(C为带有刻度的玻璃管);
④由A向B中滴加试剂至过量;
⑤待B中不再有气体产生并恢复至室温后,记录C中液面刻度,
计算得到气体的体积为V mL(经查,该气体密度为ρg/L);
⑥将B中剩余固体过滤、洗涤、干燥并称重,称得剩余固体质量为W g。
(1)A仪器的名称为___________;
(2)B中发生的反应的化学方程式为:___________;
(3)小黄在实验前将块状的铜锌合金磨成粉末状,其目的是:___________;
(4)如何检验该装置的气密性:___________;
(5)为使测得的气体体积更精确,记录C中液面刻度时,除使视线与凹液面的最低处相平外,还应___________;
(6)小黄发现实验中由于缺少某一步骤导致数据缺乏而无法计算,该步骤是:___________;
(7)通常实验前须估算药品用量,如果实验过程中,发现盐酸的量不足,应中途加酸还是重新实验:___________;理由是___________。答案:解析:(1)分液漏斗
(2)Zn+H2SO4==ZnSO4+H2↑
(3)加快反应的速率
(4)提高D管,静止片刻后,C、D液面仍存在高度差,则气密性良好
(5)使D、C中的液面相平
(6)测量铜锌合金样品的质量
(7)重新实验 中途添加酸时,会造成气体逸散,影响气体体积的精确测量 -
第15题:
为测定某铜锌合金中的铜的质量分数,某校化学兴趣小组用该合金与稀硫酸反应,进行了三次实验。所有的相关数据记录见下表(实验误差忽略不计);
(1)计算该合金中铜的质量分数;
(2)求第三次实验所得溶液中溶质的质量分数。答案:解析:
-
第16题:
以锌为主的铜合金称为()。在铜锌合金基础上再加入少量其他元素如锰、铝硅等可以构成()。
正确答案:黄铜;特殊黄铜 -
第17题:
测量一定质量的铝锌合金与强酸溶液反应产生氢气的体积,可以求得合金中铝和锌的质量分数.现有下列实验用品:中学实验常用仪器、800mL烧杯、100mL量筒、短颈玻璃漏斗、铜网、铝锌合金样品、浓盐酸(密度1.19g/cm3)、水.合金样品用铜网包裹的目的是什么?
正确答案:使样品在反应时能在烧杯底适当的位置(或答避免反应时样品漂浮). -
第18题:
属于铝合金中强度最好的是()
- A、铝铜合金
- B、铝镁合金
- C、铝锌合金
- D、铝锌镁
正确答案:D -
第19题:
在电力行业中,大部分的金属部件、设备所使用的材料为()
- A、钢铁
- B、铝及铝合金
- C、锌及锌合金
- D、铜及铜合金
正确答案:A,B,D -
第20题:
碳素钢是()合金,黄铜是铜、锌合金。
- A、铁、碳;
- B、铜、锌;
- C、铝、钢。
正确答案:A -
第21题:
轻金属通常是指()。
- A、钛及钛合金
- B、铜及铜合金
- C、锌及锌合金
- D、镍及镍合金
- E、铝及铝合金
正确答案:A,E -
第22题:
单选题碳素钢是()合金,黄铜是铜、锌合金。A铁、碳;
B铜、锌;
C铝、钢。
正确答案: C解析: 暂无解析 -
第23题:
判断题锌铝合金和铝锌合金镀层的厚度可通过中性耐盐雾实验确定,其耐盐雾性能不应小于500小时。A对
B错
正确答案: 错解析: 暂无解析
