(2)在实验室中用过氧化氢溶液和二氧化锰混合制取氧气时,其中二氧化锰起______作用,发生反应的化学方程式为_____________________________________________;
题目
(2)在实验室中用过氧化氢溶液和二氧化锰混合制取氧气时,其中二氧化锰起______作用,发生反应的化学方程式为_____________________________________________;
相似考题
更多“(2)在实验室中用过氧化氢溶液和二氧化锰混合制取氧气时,其中二氧化锰起______作用,发生反应的化 ”相关问题
-
第1题:
工业上广泛采用的大规模制取氯气的方法是( )。
A.浓硫酸与二氧化锰反应
B.电解饱和食盐水溶液
C.浓硫酸与高锰酸钾反应
D.二氧化锰、食盐与浓硫酸反应
正确答案:B
-
第2题:
阅读下列三段材料,按要求完成任务。
材料一《义务教育化学课程标准(2011年版)》关于制取氧气的内容标准:初步学习氧气的实验室制取方法。
材料二教科书的知识结构体系
绪言化学使世界变得更加绚丽多彩
第一单元走进化学世界
第二单元我们周围的空气
课题1空气
课题2氧气
课题3制取氧气
实验活动l氧气的实验室制取与性质
第三单元物质构成的奥秘
第四单元自然界的水
第五单元化学方程式
第六单元碳和碳的氧化物
第七单元燃料及其利用
第八单元金属和金属材料
第九单元溶液
第十单元酸和碱
第十一单元盐化肥
第十二单元化学与生活
材料三某版本教科书“制取氧气”所呈现的部分内容:
课题3制取氧气
在实验室里.常采用加热高锰酸钾、分解过氧化氢或加热氯酸钾的方法制取氧气。
【实验2—5】
把少量高锰酸钾装入试管中,并在试管口放一团棉花,用带有导管的塞子塞紧试管。
(1)加热试管,用排水法收集一瓶氧气(如图2—14)。
(2)把带有火星的木条伸入集气瓶中,观察有什么现象发生。
高锰酸钾是一种暗紫色的固体,它受热时,分解出氧气,同时还有锰酸钾和二氧化锰生成:
除用加热高锰酸钾的方法制取氧气外.在实验室里还常常用分解过氧化氢的方法制取氧气。过氧化氢溶液在常温下可以分解放出氧气.但是在利用过氧化氢分解制取氧气时,通常还要放入少量二氧化锰.这是为什么呢?
【探究】
分解过氧化氢制氧气的反应中二氧化锰的作用
1.实验
(1)在试管中加入5 ml 5%过氧化氢溶液,把带火星的木条伸入试管,观察现象。
(2)向上述试管中加入少量二氧化锰,把带火星的木条伸入试管。观察现象(如图2一15)。
(3)待上述试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,观察现象。待试管中又没有现象发生时,再重复上述操作.观察现象。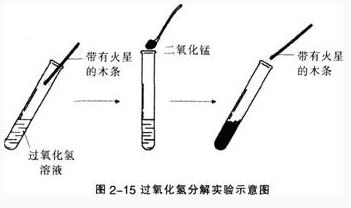
2.分析与讨论
(1)在实验(1)和(2)中木条是否复燃?发生这种现象的原因可能是什么?
(2)在实验(3)的重复实验中,反应后二氧化锰有无变化?
(3)综合分析实验(1)一(3)中所观察到的现象,你认为二氧化锰在过氧化氢分解的反应中起了什么作用?
在实验(1)中,带火星的木条不能复燃,是因为过氧化氢溶液在常温下分解缓慢.放出的氧气很少。在实验(2)中,木条复燃,是因为过氧化氢溶液中加入少量二氧化锰,使分解加速。这一反应可以表示如下:
在实验(3)中,实验重复多次,每次只消耗了过氧化氢,二氧化锰好像永远用不完。如果在实验前用精密的天平称量二氧化锰的质量,实验后把二氧化锰洗净、干燥.再称量,你会发现它的质量没有发生变化。把它再加到过氧化氢溶液中.还可以加速过氧化氢分解。这种在化学反应里能改变其他物质的化学反应速率.而本身的质量和化学性质在反应前后都没有发生变化
的物质叫作催化剂(又叫触媒)。催化剂在化学反应中所起的作用叫作催化作用。硫酸铜溶液等对过氧化氢的分解也具有催化作用。
催化剂在化工生产中具有重要而广泛的应用,生产化肥、农药、多种化工原料等都要使用催化剂。
在实验室里还可以通过加热混有二氧化锰的氯酸钾固体制取氧气.除生成氧气外,同时还有一种叫氯化钾的物质生成。二氧化锰在这一反应中也是催化剂。这个反应可表示如下:
【讨论】
分析上述三个制取氧气的反应,它们有什么共同特征?与化舍反应有什么不同?
要求:
(1)试对本课内容进行学情分析。
(2)确定本课的三维教学目标。
(3)确定本课的教学重点和难点。
(4)试对本课内容进行教学价值分析。
(5)设计本课教学内容的教学过程图。答案:解析:【知识点】化学教学设计能力——制取氧气
(1)通过前面的学习,学生对氧气的性质和用途有了较为深入的认识,对氧气产生了浓厚的探究欲望.他们渴望能亲手制得一瓶纯净的氧气。通过操控化学反应制备得到一种物质,对学生而言是一件神奇的事情。
学生对物质制备的认识仅限于从小学自然课、生活经验等途径获得的零星的、感性的体验.还不能形成系统的、理性的思考。同时,学生的化学知识、实验技能、探究能力也都处在初级阶段,对如何分析和处理实验中遇到的问题会感到束手无策。因此,氧气的实验室制法,在帮助学生顺利获得氧气的同时,要注意制备物质的思路的总结和落实。
(2)知识与技能:①知道实验室用过氧化氢、氯酸钾、高锰酸钾制取氧气的原理,能写出文字表达式:②能识别固体药品制备气体和液体药品制备气体的整套实验装置;③了解催化剂,能解释证明催化作用的对比实验;④在制备氧气的过程中,进行装置气密性检验、药品的取用、物质的加热、排水取气等基本实验操作的训练,能检验氧气的生成。
过程与方法:①通过制备氧气的过程,初步学习通过化学实验制备物质的一般思路方法;②通过催化剂作用的有关实验,进一步理解对比和变量控制的方法在化学实验中的应用。
情感态度与价值观:①通过实验活动获得氧气,感受实验成功的快乐,感受个人对自然改变的力量:②通过化学变化获得氧气,建立物质间可以转化的观念,加深化学对人类伟大贡献的理解。
(3)教学重点:氧气实验室制法的原理和装置。
教学难点:制备物质的一般思路和方法的建立。
(4)①物质制备是实验化学的重要研究内容,也是人类利用化学改变社会的重要方式,氧气实验室制法的学习是学习研究物质制备的启蒙和基础。
②氧气实验室制法涉及的两套实验装置都是实验化学气体制备的基本装置,在制备很多气体时可以应用。
③学习前.学生知道空气中有氧气,我们的身边充斥着氧气,但是他们没有获得过纯净的氧气。如果需要得到氧气,学生首先想到的是物理方法,即从空气中分离。通过学习,学生获得了纯净的氧气.虽然外观上与空气没什么不同,但是这个过程会增强学生对自然的能动感,感受到科学的力量。通过化学方法制得氧气,能够促使学生建立物质转化的观点。在制备氧气的过程中形成制备物质的思路方法,这是学生后续学习的基础以及解决制备问题的基本途径。
(5)教学流程图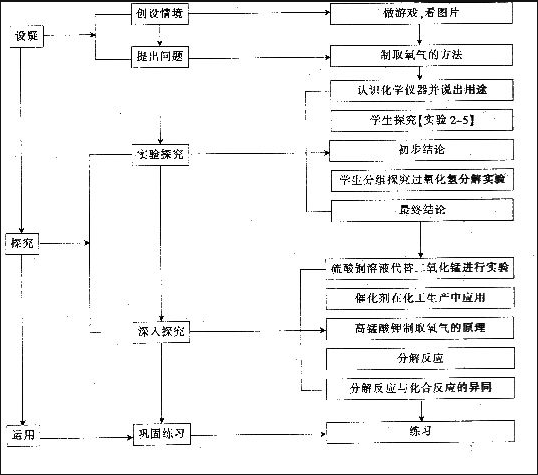
-
第3题:
【单选题】在过氧化氢溶液中加入少量二氧化锰固体时,发生以下哪种反应()。
A.过氧化氢被氧化
B.过氧化氢分解
C.过氧化氢被还原
D.复分解
B -
第4题:
下列说法中不正确的是( )
A.在过氧化氢溶液的分解反应中,二氧化锰起催化作用
B.氧气的化学性质很活泼,在常温下能与所有物质发生化学反应
C.细铁丝在氧气里燃烧时,火星四射,生成黑色固体
D.用排水法可以收集不易溶于水的气体
B -
第5题:
要证明二氧化锰在过氧化氢分解过程中起催化作用,可以设计的实验有
A.过氧化氢溶液中加与不加二氧化锰实验的比较
B.二氧化锰加热分解检验有没有氧气生成
C.在与过氧化氢反应过的二氧化锰中,继续加过氧化氢溶液
D.与过氧化氢反应过的二氧化锰质量没有变化
过氧化氢溶液中加与不加二氧化锰实验的比较;在与过氧化氢反应过的二氧化锰中,继续加过氧化氢溶液;与过氧化氢反应过的二氧化锰质量没有变化
