表示水硬度的是A.CaO(mg/L)B.MgC03(mg/L)C.CaC03(mg/L)D.CaCl2(mg/L)E.Ca(HC03)2(mg/L)
题目
表示水硬度的是
A.CaO(mg/L)
B.MgC03(mg/L)
C.CaC03(mg/L)
D.CaCl2(mg/L)
E.Ca(HC03)2(mg/L)
相似考题
更多“表示水硬度的是A.CaO(mg/L)B.MgC03(mg/L)C.CaC03(mg/L)D.CaCl2(mg/L ”相关问题
-
第1题:
酸性氧化电位水有效氯含量为( )
A.60mg/L±10 mg/L
B.50mg/L±10 mg/L
C.65mg/L±10 mg/L
D.55mg/L±10 mg/L
正确答案:A
-
第2题:
水的硬度以(mg/L)表示A.Ca(HCO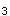 )
)
B.CaCl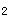
C.MgCO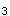
D.CaO
E.CaCO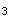 答案:E解析:
答案:E解析: -
第3题:
计算题:某地区水质分析结果如下:Ca2+:46mg/L:Mg2+:8.5mg/L;Na+:46mg/L;HCO:128.1mg/L;SO:72mg/L;CL-:49.7mg/L。试计算下列各项:(1)审核阴阳离子含量是否合理:(2)计算各种硬度值,总碱度值。
正确答案: 解:(1)各种离子的物质的量浓度为
c(1/2Ca2+)=46/20=2.3(mmol/L):
c(1/2Mg2+)=8.5/12=0.7(mmol/L)
c(HCO)=128.1/61=2.1(mmol/L)
c(1/2SO)=72/48=1.5(mmol/L)
c(Na+)=46/23=2(mmol/L)
c(CL-)=497/35.5=1.4(mmol/L)
Σc+=c(1/2Ca2+)+c(1/2Mg2+)+c(Na+)=5.0(mmol/L)
Σc-=c(HCO)+(1/2SO)+c(CL-)=5.0(mmol/L)
结果:Σc+=Σc-,说明阴阳离子含量合理。
(2)总硬度=2.3+0.7=3.0(mmol/L)
碳酸盐硬度=2.1(mmol/L)
非碳酸盐硬度=3.0-2.1=0.9(mmol/L)
全碱度=2.1(mmol/L) -
第4题:
计算题:试计算某水样的含盐量、硬度值、碱度值。已知该水样水质分析结果如下:Ca2+:30mg/L;Mg2+:6mg/L;Na+:23mg/L;Fe2+:27.9mg/L;HCO3-:122mg/L;SO42-:24mg/L;Cl-:35.5mg/L;HSiO3-:38.5mg/L。
正确答案:各种离子的物质的量的浓度为:
c(1/2Ca2+)=30/20=1.5(mmol/L)
c(1/2Mg2+)=6/12=0.5(mmol/L)
c(Na+)=23/23=1.0(mmol/L)
c(1/2Fe2+)=27.9/27.9=1.0(mmol/L)
c(HCO3-)=122/61=2.0(mmol/L)
c(1/2SO42-)=24/48=0.5(mmol/L)
c(Cl-)=35.5/35.5=1.0(mmol/L)
c(HSiO3-)=38.5/77=0.5(mmol/L)
则含盐量=Σc+=c(1/2Ca2+)+c(1/2Mg2+)+c(Na+)+c(1/2Fe2+)=1.5+0.5+1+1=4(mmol/L)
硬度=c(1/2Ca2+)+c(1/2Mg2+)=1.5+0.5=2(mmol/L)
碱度=c(HCO3-)+c(HSiO3-)=2+0.5=2.5(mmol/L)
水样的含盐量=4.0mmol/L;硬度值=2.0mmol/L;碱度值=2.5mmol/L。 -
第5题:
计算题:设某水样经水质化验,结果如下:〔Ca2+〕=86.0mg∕L,〔HCO3-〕=329.4mg∕L,〔Mg2+〕=18.0mg∕L,〔SO42-〕=19.2mg∕L,〔Na+〕=10.4mg∕L,〔Cl-〕=15.98mg∕L。试求①水样中可能组合的各化合物的含量;②水样中总硬度、碳酸盐硬度、非碳酸盐硬度、负硬、总碱度、含盐量各为多少?
正确答案: 将每种离子的含量都换算成mmol∕L单位表示:
〔Ca2+〕=86.0÷20=4.3mmol∕L
〔Mg2+〕=18.0÷12=1.5mmol∕L
〔Na+〕=10.4÷23=0.45mmol∕L
阳离子含量为6.23mmol∕L;
〔HCO3-〕=329.4÷61=5.4mmol∕L
〔SO42-〕=19.2÷48=0.4mmol∕L
〔Cl-〕=15.98÷35.5=0.45mmol∕L
阴离子含量为6.25mmol∕L。计算结果该水样中的阳离子和阴离子含量基本相等,说明计算结果正确。
①求水样中可能组合的各化合物的含量:
Ca2+先和HCO3-组合成4.3mmol∕L的Ca(HCO3)2,剩余的HCO3-和Mg2+组合成5.4-4.3=1.1mmol∕L的Mg(HCO3)2,余下的Mg2+和SO42-组合成0.4mmol∕L的MgSO4。Na+和Cl-组合成0.45mmol∕L的NaCl。经整理得出该水样中可能组合的各化合物的含量为:
碳酸氢钙(Ca(HCO3)2)4.3mmol∕L
碳酸氢镁(Mg(HCO3)2)1.1mmol∕L
硫酸镁(MgSO4)0.4mmol∕L
氯化钠(NaCl)0.45mmol∕L
②由上述计算结果可以得知,该水样中碳酸盐硬度为5.4mmol∕L,非碳酸盐硬度为0.4mmol∕L,总硬度为5.8mmol∕L。总碱度为5.4mmol∕L。该水样属于Ca2++Mg2+>HCO3-,即总硬度大于总碱度的永硬水,既有暂时硬度,又有永久硬度。又因Mg2+<HCO3-,该水样属于镁硬水,水样中有镁的碳酸盐硬度,而没有钙的非碳酸盐硬度。同时,由化验结果得知该水样的含盐量为478.98mg∕L。
①该水样中可能组合的各化合物的含量为:碳酸氢钙(Ca(HCO3)2)4.3mmol∕L,碳酸氢镁(Mg(HCO3)2)1.1mmol∕L,硫酸镁(MgSO4)0.4mmol∕L,氯化钠(NaCl)0.45mmol∕L。
②该水样中碳酸盐硬度为5.4mmol∕L,非碳酸盐硬度为0.4mmol∕L,总硬度为5.8mmol∕L。无负硬度。总碱度为5.4mmol∕L。含盐量为478.98mg∕L。 -
第6题:
正常血钾值的范围为()
- A、2.5mg/L~3.5mg/L
- B、3.5mg/L~5.5mg/L
- C、3.5mg/L~5.5mg/L
- D、2.5mg/L~3.5mg/L
- E、25mg/L~35mg/L
正确答案:C -
第7题:
某地区水质分析结果如下:〔Ca2+〕=46.0mg∕L,〔HCO3-〕=128.1mg∕L,〔Mg2+〕=8.5mg∕L,〔SO42-〕=72.0mg∕L,〔Na+〕=46.0mg∕L,〔Cl-〕=49.7mg∕L。试求①审核阴、阳离子含量是否合理;②水中的总硬度和总碱度;③判断该水属于何种水;④水中的碳酸盐硬度、非碳酸盐硬度、负硬度;⑤写出假想化合物的分子式,并计算其含量。
正确答案:
①将每种离子的含量都换算成mmol∕L单位表示:
〔Ca2+〕=46.0∕20=2.3mmol∕L
〔Mg2+〕=8.5∕12=0.7mmol∕L
〔Na+〕=46.0∕23=2.0mmol∕L
阳离子含量为5.0mmol∕L;
〔HCO3-〕=128.1∕61=2.1mmol∕L
〔SO42-〕=72.0∕48=1.5mmol∕L
〔Cl-〕=49.7∕35.5=1.4mmol∕L阴离子含量为5.0mmol∕L。计算结果该水样中的阳离子和阴离子各为5.0mmol∕L,彼此相等,说明计算结果正确。
②水中的总硬度和总碱度分别为:
YD=〔Ca2+〕+〔Mg2+〕=2.3+0.7=3.0mmol∕L
JD=〔HCO3-〕=2.1mmol∕L
③由于该水样的总硬度YD大于总碱度JD,即Ca2++Mg2+>HCO3-,可知该水属于非碱性水。水中既有碳酸盐硬度,又有非碳酸盐硬度,无负硬度。又因〔Ca2+〕>〔HCO3-〕,可知该水为钙硬水,水中有钙的非碳酸盐硬度(即CaSO4),没有镁的碳酸盐硬度。
④水中的碳酸盐硬度、非碳酸盐硬度、负硬度分别为:
YDT=JD=3.0mmol∕L
YDFT=YD-JD=3.0-2.1=0.9mmol∕L
YDf=0
⑤阴、阳离子组合成各种假想化合物的组成、想化合物的分子式及其含量:
Ca2+先和HCO3-结合成2.1mmol∕L的Ca(HCO3)2,剩余的Ca2+和SO42-结合成2.3-2.1=0.2mmol∕L的CaSO4,Mg2+和剩余的SO42-结合成0.7mmol∕L的MgSO4,Na+和余下的SO42-结合成1.5-0.2-0.7=0.6mmol∕L的Na2SO4,余下的Na+和Cl-结合成0.6mmol∕L的NaCl。
①水中阴、阳离子含量合理;②水中的总硬度和总碱度分别为3.0mmol∕L和2.1mmol∕L;③该水属于非碱性水,且为钙硬水;④水中的碳酸盐硬度、非碳酸盐硬度、负硬度分别为3.0mmol∕L、0.9mmol∕L和0:⑤水中离子假想结合化合物为:
Ca(HCO3)2(碳酸氢钙)2.1mmol∕L
CaSO4(硫酸钙)0.2mmol∕L
MgSO4(硫酸镁)0.7mmol∕L
Na2SO4(硫酸钠)0.6mmol∕L
NaCl(氯化钠)0.6mmol∕L -
第8题:
计算题:试计算某水样的含盐量、硬度值、碱度值。已知水样水质分析结果如下:Ca2+:30mg/L;Mg2+:6mg/L:Na+:23mg/L:Fe2+:27.9mg/L:HCO:122mg/L:SO:24mg/L:CL-:35.5mg/L;HSiO:38.5mg/L。
正确答案: 解:各种离子的物质的量的浓度为:
c(1/2Ca2+)=30/20=1.5(mmol/L)
c(1/2Mg2+)=6/12=0.5(mmol/L)
c(1/2Fe2+)=27.9/27.9=1(mmol/L)
c(1/2HCO)=122/61=2(mmol/L)
c(1/2SO)=24/48=0.5(mmol/L)
c(1/2Na+)=23/23=1(mmoL/l)
c(CL-)=35.5/35.5=1(mmoL/L)
c(HSiO)=38.5/77=0.5(mmol/L)
则含盐量=ΣC+=c(1/2Ca2+)+c(1/2Mg2+)+c(Na+)+c(1/2Fe2+)=1.5+0.5+1+1=4(mmol/L)
硬度=c(1/2Ca2+)+c(1/2Mg2+)=1.5+0.5=2(mmol/L)
碱度=C(HCO)+c(HSiO)=2+0.5+2.5(mmol/L)
该水样的含盐量为4mmol/L,硬度为2mmol/L,碱度为2.5mmol/L。 -
第9题:
水的硬度有用mg·L-1CaO表示的,还有用硬度数表示的(每升水中含10mgCaO为1度)。今吸取水样100mL用0.0100mol·L-1EDTA溶液测定硬度,用去2.41mL计算水的硬度:用mg·L-1CaO表示();用硬度数表示()。
正确答案:13.5mg·L-1CaO;1.35°(度) -
第10题:
单选题表示水硬度的是()。ACaO(mg/L)
BMgCO3(mg/L)
CCaCO3(mg/L)
DCaCl2(mg/L)
ECa(HCO3)2(mg/L)
正确答案: E解析: 水的硬度主要取决于水中钙、镁离子的含量通常用氧化钙或者是碳酸钙的质量浓度来表示。 -
第11题:
问答题某地区水质分析结果如下:〔Ca2+〕=46.0mg∕L,〔HCO3-〕=128.1mg∕L,〔Mg2+〕=8.5mg∕L,〔SO42-〕=72.0mg∕L,〔Na+〕=46.0mg∕L,〔Cl-〕=49.7mg∕L。试求①审核阴、阳离子含量是否合理;②水中的总硬度和总碱度;③判断该水属于何种水;④水中的碳酸盐硬度、非碳酸盐硬度、负硬度;⑤写出假想化合物的分子式,并计算其含量。正确答案:
①将每种离子的含量都换算成mmol∕L单位表示:
〔Ca2+〕=46.0∕20=2.3mmol∕L
〔Mg2+〕=8.5∕12=0.7mmol∕L
〔Na+〕=46.0∕23=2.0mmol∕L
阳离子含量为5.0mmol∕L;
〔HCO3-〕=128.1∕61=2.1mmol∕L
〔SO42-〕=72.0∕48=1.5mmol∕L
〔Cl-〕=49.7∕35.5=1.4mmol∕L阴离子含量为5.0mmol∕L。计算结果该水样中的阳离子和阴离子各为5.0mmol∕L,彼此相等,说明计算结果正确。
②水中的总硬度和总碱度分别为:
YD=〔Ca2+〕+〔Mg2+〕=2.3+0.7=3.0mmol∕L
JD=〔HCO3-〕=2.1mmol∕L
③由于该水样的总硬度YD大于总碱度JD,即Ca2++Mg2+>HCO3-,可知该水属于非碱性水。水中既有碳酸盐硬度,又有非碳酸盐硬度,无负硬度。又因〔Ca2+〕>〔HCO3-〕,可知该水为钙硬水,水中有钙的非碳酸盐硬度(即CaSO4),没有镁的碳酸盐硬度。
④水中的碳酸盐硬度、非碳酸盐硬度、负硬度分别为:
YDT=JD=3.0mmol∕L
YDFT=YD-JD=3.0-2.1=0.9mmol∕L
YDf=0
⑤阴、阳离子组合成各种假想化合物的组成、想化合物的分子式及其含量:
Ca2+先和HCO3-结合成2.1mmol∕L的Ca(HCO3)2,剩余的Ca2+和SO42-结合成2.3-2.1=0.2mmol∕L的CaSO4,Mg2+和剩余的SO42-结合成0.7mmol∕L的MgSO4,Na+和余下的SO42-结合成1.5-0.2-0.7=0.6mmol∕L的Na2SO4,余下的Na+和Cl-结合成0.6mmol∕L的NaCl。
①水中阴、阳离子含量合理;②水中的总硬度和总碱度分别为3.0mmol∕L和2.1mmol∕L;③该水属于非碱性水,且为钙硬水;④水中的碳酸盐硬度、非碳酸盐硬度、负硬度分别为3.0mmol∕L、0.9mmol∕L和0:⑤水中离子假想结合化合物为:
Ca(HCO3)2(碳酸氢钙)2.1mmol∕L
CaSO4(硫酸钙)0.2mmol∕L
MgSO4(硫酸镁)0.7mmol∕L
Na2SO4(硫酸钠)0.6mmol∕L
NaCl(氯化钠)0.6mmol∕L解析: 暂无解析 -
第12题:
问答题计算题:水质资料如下: 〔Ca2+〕=56.0mg∕L,〔Mg2+〕=14.4mg∕L,〔Na+〕=46.0mg∕L; 〔HCO3-〕=335.5mg∕L,〔SO42-〕=9.6mg∕L,〔Cl-〕=10.65mg∕L。 试求①水中可能组合的各化合物的含量;②水中硬度、碳酸盐硬度、非碳酸盐硬度、负硬、碱度各为多少?正确答案: 将每种离子的含量都换算成mmol∕L单位表示:
〔Ca2+〕=56.0÷20=2.8mmol∕L
〔Mg2+〕=14.4÷12=1.2mmol∕L
〔Na+〕=46.0÷23=2.0mmol∕L
阳离子含量为6.0mmol∕L;
〔HCO3-〕=335.5÷61=5.5mmol∕L
〔SO42-〕=9.6÷48=0.2mmol∕L
〔Cl-〕=35.5÷35.5=0.3mmol∕L
阴离子含量为6.0mmol∕L。计算结果该水样中的阳离子和阴离子各为6.0mmol∕L,彼此相等,说明计算结果正确。
①水中可能组合的各化合物的含量:
Ca2+先和HCO3-结合成2.8mmol∕L的Ca(HCO3)2,剩余的HCO3-和Mg2+结合成1.2mmol∕L的Mg(HCO3)2,余下的HCO3-和Na+结合成5.5-2.8-1.2=1.5mmol∕L的NaHCO3,剩余的Na+和SO42-结合成0.2mmol∕L的Na2SO4,余下的Na+和Cl-结合成2.0-1.5-0.2=0.3mmol∕L的NaCl。经整理得出如下结果:
该水样中可能组合的各化合物的含量为:
碳酸氢钙(Ca(HCO3)2)2.8mmol∕L
碳酸氢镁(Mg(HCO3)2)1.2mmol∕L
重碳酸钠(NaHCO3)1.5mmol∕L
硫酸钠(Na2SO4)0.2mmol∕L
氯化钠(NaCl)0.3mmol∕L
②水中硬度、碳酸盐硬度、非碳酸盐硬度、负硬、碱度各为多少
该水样的硬度为YD=〔Ca2+〕+〔Mg2+〕=2.8+1.2=4.0mmol∕L;碱度为JD=〔HCO3-〕=5.5mmol∕L。可见JD>YD,即〔HCO3-〕>〔Ca2+〕+〔Mg2+〕,该水样的特征是碱度大于硬度的碱性水。Ca2+和Mg2+都成为碳酸氢盐,没有非碳酸盐硬度,有Na+的碳酸氢盐。
碳酸盐硬度YDT=YD=4.0mmol∕L
负硬度YDf=JD-YD=5.5-4.0=1.5mmol∕L
①该水样中可能组合的各化合物的含量为:碳酸氢钙(Ca(HCO3)2)2.8mmol∕L,碳酸氢镁(Mg(HCO3)2)1.2mmol∕L,重碳酸钠(NaHCO3)1.5mmol∕L,硫酸钠(Na2SO4)0.2mmol∕L,氯化钠(NaCl)0.3mmol∕L。
②水中硬度为4.0mmol∕L,碳酸盐硬度为4.0mmol∕L,没有非碳酸盐硬度,负硬为1.5mmol∕L,碱度为5.5mmol∕L。解析: 暂无解析 -
第13题:
表示水硬度的是
A.CaO(mg/L)
B.MgCO3(mg/L)
C.CaCO3(mg/L)
D.CaC12(mg/L)
E.Ca(HCO3)2(mg/L)
正确答案:C
-
第14题:
酸性氧化电位水有效氯含量为()。
- A、60mg/L±10mg/L
- B、50mg/L±10mg/L
- C、65mg/L±10mg/L
- D、55mg/L±10mg/L
正确答案:A -
第15题:
当原水()的水,可采用一级钠离子交换软化系统。
- A、含盐量<500mg/L,硬度<3mmol/L,碱度<2mmol/L
- B、含盐量<300mg/L,硬度<5mmol/L,碱度<2mmol/L
- C、含盐量<500mg/L,硬度<5mmol/L,碱度<2mmol/L
- D、含盐量<500mg/L,硬度<5mmol/L,碱度<5mmol/L
正确答案:C -
第16题:
取水样100mL,用C(EDTA)=0.0200mol/L,标准溶液测定水的总硬度,用去4.00毫升,计算水的总硬度是()(用CaCO3mg/L表示)。
- A、20mg/L
- B、40mg/L
- C、60mg/L
- D、80mg/L
正确答案:D -
第17题:
表示水硬度的是()。
- A、CaO(mg/L)
- B、MgCO3(mg/L)
- C、CaCO3(mg/L)
- D、CaCl2(mg/L)
- E、Ca(HCO3)2(mg/L)
正确答案:C -
第18题:
计算题:水质资料如下: 〔Ca2+〕=56.0mg∕L,〔Mg2+〕=14.4mg∕L,〔Na+〕=46.0mg∕L; 〔HCO3-〕=335.5mg∕L,〔SO42-〕=9.6mg∕L,〔Cl-〕=10.65mg∕L。 试求①水中可能组合的各化合物的含量;②水中硬度、碳酸盐硬度、非碳酸盐硬度、负硬、碱度各为多少?
正确答案: 将每种离子的含量都换算成mmol∕L单位表示:
〔Ca2+〕=56.0÷20=2.8mmol∕L
〔Mg2+〕=14.4÷12=1.2mmol∕L
〔Na+〕=46.0÷23=2.0mmol∕L
阳离子含量为6.0mmol∕L;
〔HCO3-〕=335.5÷61=5.5mmol∕L
〔SO42-〕=9.6÷48=0.2mmol∕L
〔Cl-〕=35.5÷35.5=0.3mmol∕L
阴离子含量为6.0mmol∕L。计算结果该水样中的阳离子和阴离子各为6.0mmol∕L,彼此相等,说明计算结果正确。
①水中可能组合的各化合物的含量:
Ca2+先和HCO3-结合成2.8mmol∕L的Ca(HCO3)2,剩余的HCO3-和Mg2+结合成1.2mmol∕L的Mg(HCO3)2,余下的HCO3-和Na+结合成5.5-2.8-1.2=1.5mmol∕L的NaHCO3,剩余的Na+和SO42-结合成0.2mmol∕L的Na2SO4,余下的Na+和Cl-结合成2.0-1.5-0.2=0.3mmol∕L的NaCl。经整理得出如下结果:
该水样中可能组合的各化合物的含量为:
碳酸氢钙(Ca(HCO3)2)2.8mmol∕L
碳酸氢镁(Mg(HCO3)2)1.2mmol∕L
重碳酸钠(NaHCO3)1.5mmol∕L
硫酸钠(Na2SO4)0.2mmol∕L
氯化钠(NaCl)0.3mmol∕L
②水中硬度、碳酸盐硬度、非碳酸盐硬度、负硬、碱度各为多少
该水样的硬度为YD=〔Ca2+〕+〔Mg2+〕=2.8+1.2=4.0mmol∕L;碱度为JD=〔HCO3-〕=5.5mmol∕L。可见JD>YD,即〔HCO3-〕>〔Ca2+〕+〔Mg2+〕,该水样的特征是碱度大于硬度的碱性水。Ca2+和Mg2+都成为碳酸氢盐,没有非碳酸盐硬度,有Na+的碳酸氢盐。
碳酸盐硬度YDT=YD=4.0mmol∕L
负硬度YDf=JD-YD=5.5-4.0=1.5mmol∕L
①该水样中可能组合的各化合物的含量为:碳酸氢钙(Ca(HCO3)2)2.8mmol∕L,碳酸氢镁(Mg(HCO3)2)1.2mmol∕L,重碳酸钠(NaHCO3)1.5mmol∕L,硫酸钠(Na2SO4)0.2mmol∕L,氯化钠(NaCl)0.3mmol∕L。
②水中硬度为4.0mmol∕L,碳酸盐硬度为4.0mmol∕L,没有非碳酸盐硬度,负硬为1.5mmol∕L,碱度为5.5mmol∕L。 -
第19题:
硬度的单位符号用()表示。
- A、mg/L;
- B、mmol/L;
- C、S/cm;
- D、mN/L
正确答案:B -
第20题:
计算题:根据下列水质的分析结果计算;(1)阴阳离子含量是否确:(2)各类硬度值。 Ca2+:54mg/L;HCO:170.8mg/L;Mg2+:9.6mg/L;SO:43.2mg/L:Na+:11.5mg/L:CL-:10.65mg/L;
正确答案: 解:(1)各种离子的物质的量浓度为
c(1/2Ca2+)=54/20=2.7(mmol/L)
c(1/2Mg2+)=9.6/12=0.8(mmol/L)
c(HCO)=170.8/61=2.8(mmol/L)
c(1/2SO)=43.2/48=0.9(mmol/L)
c(Na+)=11.5/23=0.5(mmol/L)
c(CL-)=10.65/35.5=0.3(mmol/L)
Σc+=c(1/2Ca2+)+c(1/2Mg2+)+c(Na+)=4.0(mmol/L)
Σc-=c(HCO)+c(1/2SO)+c(CL-)=4.0(mmol/L)
结果:Σc+=Σc-,说明阴阳离子含量合理。
(2)总硬度=2.7+0.8=3.5(mmol/L)
碳酸盐硬度=2.8(mmol/L)
非碳酸硬度=3.5-2.8=0.7(mmol/L) -
第21题:
问答题分析人员测定某项目的单个空白值20次,其测定值分别为0.006mg/L、0.006mg/L、0.010mg/L、0.015mg/L、0.011mg/L、0.010mg/L、0.010mg/L、0.010mg/L、0.013mg/L、0.015mg/L、0.015mg/L、0.015mg/L、0.012mg/L、0.014mg/L、0.010mg/L、0.005mg/L、0.005mg/L、0.012mg/L、0.012mg/L、0.005mg/L,请计算出该空白质控图的平均值、标准偏差、上控制限、上警告限和上辅助限。正确答案: X.平均=0.011mg/l
标准偏差Sb=0.004mg/l
上控制限X平均+3Sb=0.023mg/l
上警告限X平均+2Sb=0.019mg/l
上辅助限X平均+Sb=0.015mg/l解析: 暂无解析 -
第22题:
单选题自来水的总硬度()。A≢450mg/L
B≢400mg/L
C≢350mg/L
D≢300mg/L
正确答案: B解析: 暂无解析 -
第23题:
问答题计算题:设某水样经水质化验,结果如下:〔Ca2+〕=86.0mg∕L,〔HCO3-〕=329.4mg∕L,〔Mg2+〕=18.0mg∕L,〔SO42-〕=19.2mg∕L,〔Na+〕=10.4mg∕L,〔Cl-〕=15.98mg∕L。试求①水样中可能组合的各化合物的含量;②水样中总硬度、碳酸盐硬度、非碳酸盐硬度、负硬、总碱度、含盐量各为多少?正确答案: 将每种离子的含量都换算成mmol∕L单位表示:
〔Ca2+〕=86.0÷20=4.3mmol∕L
〔Mg2+〕=18.0÷12=1.5mmol∕L
〔Na+〕=10.4÷23=0.45mmol∕L
阳离子含量为6.23mmol∕L;
〔HCO3-〕=329.4÷61=5.4mmol∕L
〔SO42-〕=19.2÷48=0.4mmol∕L
〔Cl-〕=15.98÷35.5=0.45mmol∕L
阴离子含量为6.25mmol∕L。计算结果该水样中的阳离子和阴离子含量基本相等,说明计算结果正确。
①求水样中可能组合的各化合物的含量:
Ca2+先和HCO3-组合成4.3mmol∕L的Ca(HCO3)2,剩余的HCO3-和Mg2+组合成5.4-4.3=1.1mmol∕L的Mg(HCO3)2,余下的Mg2+和SO42-组合成0.4mmol∕L的MgSO4。Na+和Cl-组合成0.45mmol∕L的NaCl。经整理得出该水样中可能组合的各化合物的含量为:
碳酸氢钙(Ca(HCO3)2)4.3mmol∕L
碳酸氢镁(Mg(HCO3)2)1.1mmol∕L
硫酸镁(MgSO4)0.4mmol∕L
氯化钠(NaCl)0.45mmol∕L
②由上述计算结果可以得知,该水样中碳酸盐硬度为5.4mmol∕L,非碳酸盐硬度为0.4mmol∕L,总硬度为5.8mmol∕L。总碱度为5.4mmol∕L。该水样属于Ca2++Mg2+>HCO3-,即总硬度大于总碱度的永硬水,既有暂时硬度,又有永久硬度。又因Mg2+<HCO3-,该水样属于镁硬水,水样中有镁的碳酸盐硬度,而没有钙的非碳酸盐硬度。同时,由化验结果得知该水样的含盐量为478.98mg∕L。
①该水样中可能组合的各化合物的含量为:碳酸氢钙(Ca(HCO3)2)4.3mmol∕L,碳酸氢镁(Mg(HCO3)2)1.1mmol∕L,硫酸镁(MgSO4)0.4mmol∕L,氯化钠(NaCl)0.45mmol∕L。
②该水样中碳酸盐硬度为5.4mmol∕L,非碳酸盐硬度为0.4mmol∕L,总硬度为5.8mmol∕L。无负硬度。总碱度为5.4mmol∕L。含盐量为478.98mg∕L。解析: 暂无解析
