PCl5、PCl3、Cl2构成的体系中,如果存在如下化学反应PCl5(气)=PCl3(气)+Cl2(气)则该体系的组分数为2。
题目
PCl5、PCl3、Cl2构成的体系中,如果存在如下化学反应PCl5(气)=PCl3(气)+Cl2(气)则该体系的组分数为2。
相似考题
更多“PCl5、PCl3、Cl2构成的体系中,如果存在如下化学反应PCl5(气)=PCl3(气)+Cl2(气)则该体系的组分数为2。”相关问题
-
第1题:
对于可逆反应:PCl5(g)===PCl3(g)+Cl2(g),下列说法正确的是:( )A.恒温下,增大压力,由于产物分子数多,Kc值减小,平衡逆向移动
B.升高温度,反应速度加快,PCl5的分解率增大
C.减小总压力,反应速度减慢,PCl5转化率降低
D.降低温度,PCl5的分解率降低,此反应为吸热反应答案:D解析: -
第2题:
反应 ,此温度下平衡时, 如p(PCl5)=p(PCl3),则p(C12)等于:
A. 130. 38kPa
,此温度下平衡时, 如p(PCl5)=p(PCl3),则p(C12)等于:
A. 130. 38kPa
B. 0. 767kPa
C. 7607kPa
D. 7. 67X10-3kPa答案:A解析:
-
第3题:
由TiO2制备TiCl4可用下列哪种方法()
- A、把TiO2溶于稀HCl
- B、把TiO2溶于热的浓HCl
- C、加热TiO2和C的混合物,并通入Cl2气
- D、加热TiO2,并通入Cl2气
正确答案:C -
第4题:
在一定温度和压强下,某一定量的PCl5和Cl2。试判断在下列情况下,PCl5的离解度是增大还是减小。 (1) 减压使PCl5的体积变为2dm-3; (2) 保持压强不变,加入氮气,使体积增至2dm3; (3) 保持体积不变,加入氮气,使压强增加1倍; (4) 保持压强不变,加入氮气,使体积变为2dm3; (5) 保持压强不变,加入氮气,使压强增加1倍。
正确答案: (1)增大;
(2)增大;
(3)不变;
(4)减小;
(5)减小 -
第5题:
热导式氢分析器在分析工艺样气时,如样气中含有()气体时,则测量结果偏高。
- A、CH4
- B、N2
- C、N2O
- D、Cl2
正确答案:A -
第6题:
PCl5(g) = PCl3(g) + Cl2(g),在一定T和P下,若一定量的PCl5气体的体积为1升,此时PCl5气体已有50%分解为PCl3和 Cl2。若减少压力使体积变为2升,则PCl5的分解率将(),若保持压力不变,加入氦气,使体积变为2,则PCl5的分解率将()。(填“增大”、“减少”、“不变”)
正确答案:增大;增大 -
第7题:
PCl5的分解反应:PCl5(g)=PCl3(g)+Cl2(g),2000C达到平衡时有48.5%分解,3000C达到平衡时有97%分解。则下列说法正确的是()
- A、此反应为放热反应
- B、反应是吸热反应
- C、升高温度,平衡逆向移动
- D、压力改变对平衡无影响
正确答案:B -
第8题:
当反应PCl5(g)=PCl3(g)+Cl2(g)达平衡时,增大系统总压力,平衡()移动。
正确答案:向左 -
第9题:
对于化学反应:Cl2+6NaOHNaClO3+5NaCl+3H2O,下列评述中,Cl2在该反应中所起的作用的正确评述是()。
- A、Cl2既是氧化剂,又是还原剂
- B、Cl2是氧化剂,不是还原剂
- C、Cl2是还原剂,不是氧化剂
- D、Cl2既不是氧化剂,又不是还原剂
正确答案:A -
第10题:
在250℃,PCl5全部气化,并能部分解离为PCl3(g)和Cl2(g)。将4.16gPCl5置于1.00L容器中,在250℃全部气化之后,测定其总压力为113kPa,那么其中包含的气体有();它们的分压是()。
正确答案:pPCl5=60.8kPa;pCl2=pPCl3=26.1kPa -
第11题:
当反应 PCl5(g) = PCl3(g) + Cl2(g) 达平衡时,加入惰性气体,但维持系统总压力不变,平衡()移动。
正确答案:向右 -
第12题:
单选题反应PCl3(g)+Cl2(g)PC5(g),在298K时,,此温度下平衡时,如p(PCl5)=p(PCl3),则p(Cl2)=()。A130.38kPa
B0.767kPa
C7607kPa
D7.67×10-3kPa
正确答案: A解析: 暂无解析 -
第13题:
反应 此温度下平衡时,如p(PCl5)=p(PCl3),则p(Cl2)等于:
A. 130. 38kPa
此温度下平衡时,如p(PCl5)=p(PCl3),则p(Cl2)等于:
A. 130. 38kPa
B. 0. 767kPa
C. 760 7kPa
D.7.67X10-3kPa答案:A解析: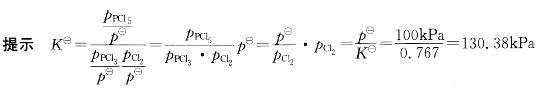
-
第14题:
Cl2的临界温度为144℃,临界压力为7.7MPa。在308K下,某装有Cl2的钢瓶中Cl2的压力为6200kPa,此钢瓶中的Cl2必为()。A.气态
B.液态
C.气、液两相平衡
D.气、液不分的状态答案:C解析: -
第15题:
在273℃时,向真空容器中引人五氯化磷,此时容器中压力为1atm 测得气体的密度为2.48g/L,试从这些数据计算PCl5(g)←→PCl3(g)+ Cl2(g)的Kp和Kc及各平衡物质的分压。
正确答案: Kp=3.3(atm); Kc=0.074(mol/L); Pc12=Ppc13=0.47atm; Ppc15=0.06atm. -
第16题:
欲除去Cl2中少量HCl气体,可将此混合气体通过饱和食盐水的洗气瓶。
正确答案:正确 -
第17题:
对反应PCl3(g)+Cl2(g)=PCl5(g),减小总压能提高PCl3/sub>的转化率。
正确答案:错误 -
第18题:
反应 PCl5(g) = PCl3(g) + Cl2(g),平衡时总压力为Pθ (Pa),离解率为50%。则此时的Kθ为()
- A、1
- B、1/2
- C、1/3
- D、1/4
正确答案:C -
第19题:
在一定温度和压强下,某一定量的PCl5气体体积为1L,此时PCl5已经有50%离解为PCl3和Cl2,试判断在下列情况下,PCl5的离解度是增加还是减少? (1)减少压强,使PCl5的体积变为2L; (2)保持压强不变,加入氮气,使体积增加至2L; (3)保持体积不变,加入氮气,使压强增加1倍; (4)保持压强不变,加入氯气,使体积变为2L; (5)保持体积不变,加入氯气,使压强增加1倍。
正确答案: (1)增加
(2)增加
(3)不变
(4)减小
(5)减小 -
第20题:
反应PCl3(g)+Cl2(g)PC5(g),在298K时,,此温度下平衡时,如p(PCl5)=p(PCl3),则p(Cl2)=()。
- A、130.38kPa
- B、0.767kPa
- C、7607kPa
- D、7.67×10-3kPa
正确答案:A -
第21题:
在某温度下,一密闭的刚性容器中的PCl5(g)达到分解平衡,若往此容器中充入N2(g)使体系压力增大二倍(此时体系仍可按理想气体处理),则PCl5(g)的离解度将:()
- A、增大
- B、减小
- C、不变
- D、视温度而定
正确答案:C -
第22题:
下列反应中△rSm值最大的是()
- A、PCl5(g)→PCl3(g)+Cl2(g)
- B、2SO2(g)+O2(g)→2SO3(g)
- C、3H2(g)+N2(g)→2NH3(g)
- D、C2H6(g)+3.5O2(g)→2CO2(g)+3H2O(l)
正确答案:A -
第23题:
Li - Cl2电池结构如下: Li│LiCl((饱和液)有机溶剂)│Cl2(pθ)│Pt已知ΔfGmθ[LiCl(s)]=-384kJ/mol,则该电池的电动势值E为:()
- A、1V
- B、2V
- C、3V
- D、4V
正确答案:D
