某温度时,已知0.100mol/dm3氢氰酸(HCN)的电离度为0. 010%,该温度时HCN的标准电离常数是: A. 1.0X10-5 B. 1.0X10-4 C. 1.0X10-9 D. 1.0X10-6
题目
 是:
是:
B. 1.0X10-4
C. 1.0X10-9
D. 1.0X10-6
相似考题
更多“某温度时,已知0.100mol/dm3氢氰酸(HCN)的电离度为0. 010%,该温度时HCN的标准电离常数是: ”相关问题
-
第1题:
已知某一元弱酸的浓度为0. 010mol/L,pH=4. 55,则其电离常数为:A. 5. 8X10-2
B.9. 8X10-3
C.8. 6X10-7
D. 7. 9X10-8答案:D解析:
-
第2题:
在某温度时,已知0.100 mol/dm3的氢氰酸(HCN)的电离度为0.010%,该温度时HCN的标准电离常数 是:
是:
(A)1.0 ×10?5
(B)1.0 ×10?4
(C)1.0 ×10?9
(D)1.0 ×10?6答案:C解析:
-
第3题:
强电解质的特点是()
- A、溶液的导电能力较强
- B、在溶液中存在电离平衡
- C、在溶液中不存在分子,完全电离为离子
- D、温度一定,电离常数一定
- E、一般浓度时电离度较小
正确答案:A,C -
第4题:
一定温度下,HCN=H++CN-在稀溶液中建立平衡,减少HCN电离度的方法是()。
- A、加水
- B、升温
- C、加压
- D、加入适量NaCN
正确答案:D -
第5题:
弱酸的电离常数Ka与该酸的浓度无关,只随温度变化。
正确答案:正确 -
第6题:
已知:Kθ(HCN)=6.2×10-10,Kθ(NH3·H2O)=1.8×10-5。则反应NH3+HCN→NH4++CN-的标准平衡常数等于()。
- A、0.90
- B、1.1
- C、9.0×10-5
- D、9.0×10-19
正确答案:B -
第7题:
已知0.10mol.L-1HAc其[H+]=1.3×10-3mol.L-1 ,则HAc的电离度为(),电离平衡常数为()。
正确答案:1.3﹪;1.69×10-5 -
第8题:
在0.05mol/L的HCN中,若有0.01%的HCN电离了,则HCN的解离常数Ka为()。
- A、5×10-8
- B、5×10-10
- C、5×10-6
- D、2.5×10-7
正确答案:B -
第9题:
在某温度时,下列溶液体系中属缓冲溶液的是:()
- A、0.100mol/dm3的NH4Cl溶液
- B、0.100mol/dm3的NaAC溶液
- C、0.400mol/dm3的HCl与0.200mol/dm的NH3·H2O等体积混合后的溶液
- D、0.400mol/dm3的NH3H2O与0.200mol/dm3的HCL等体积混合后的溶液
正确答案:D -
第10题:
单选题在0.05mol/L的HCN中,若有0.01%的HCN电离了,则HCN的解离常数Ka为()。A5×10-8
B5×10-10
C5×10-6
D2.5×10-7
正确答案: C解析: 暂无解析 -
第11题:
单选题关于电离平衡常数,下面说法正确的是()。A是电离度两倍;
B是已电离阴、阳离子浓度之积与分子浓度之比;
C与溶液的浓度有关;
D与溶液的温度无关
正确答案: B解析: 暂无解析 -
第12题:
单选题某酸在18℃时的平衡常数为1.84×10-5,在25℃时的平衡常数为1.87×10-5,则说明该酸()。A在18℃时溶解度比25℃时小
B电离是一个放热过程
C温度高时电离度变大
D温度低时溶液中的氢离子浓度变大
正确答案: A解析: 暂无解析 -
第13题:
在0.05mol/dm3的HCN中,若有0.01%的HCN电离子,则HCN的解离常数为( )。 答案:A解析:
答案:A解析: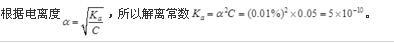
-
第14题:
某温度时,已知0.100mol/dm3氢氰酸(HCN)的电离度为0. 010%,该温度时HCN的标准电离常数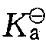 是:
是:
A. 1.0X10-5 B. 1.0X10-4 C. 1.0X10-9 D. 1.0X10-6答案:C解析:提示:电离度α与电离常数的关系:Ka =Cα2/(1-α)。 -
第15题:
电离常数K表示弱电解质电离的能力,K愈小,表示电离程度愈()K随温度升高而()
正确答案:小;增大 -
第16题:
某酸在18℃时的平衡常数为1.84×10-5,在25℃时的平衡常数为1.87×10-5,则说明该酸()。
- A、在18℃时溶解度比25℃时小
- B、的电离是一个吸热过程
- C、温度高时电离度变小
- D、温度高时溶液中的氢离子浓度变小
正确答案:B -
第17题:
关于电离平衡常数,下面说法正确的是()。
- A、是电离度两倍;
- B、是已电离阴、阳离子浓度之积与分子浓度之比;
- C、与溶液的浓度有关;
- D、与溶液的温度无关
正确答案:B -
第18题:
已知在298015K时,下列反应的标准平衡常数: HCN=H++CN- Kθa=4.93×10-10 NH3+H2O = NH4+ +OH- Kθb=4.93×10-10 H2O = H++OH- Kθw=4.93×10-10 下列反应的标准平衡常数Kθ是() NH3 + HCN = NH4++CN-
- A、8.82×10-29
- B、2.75×10-19
- C、8.82×10-1
正确答案:C -
第19题:
在0.05mol·L-1HCN溶液中,若有0.01%的HCN解离,则HCN的平衡常数为()。
- A、5*10-10
- B、5*10-8
- C、5*10-6
- D、5*10-7
正确答案:A -
第20题:
HCN的解离常数Ka=4.9×10-10,0.010mol·L-1的HCN溶液,其解离度为()。
- A、2.2×10-4
- B、0.022%
- C、2.2×10-5
- D、0.0022%
正确答案:B -
第21题:
单选题在0.05mol·dm-3的HCN溶液中,若有0.01%的HCN电离了,则HCN的电离常数为:()A5×10-12
B5×10-8
C5×10-5
D5×10-10
正确答案: A解析: 暂无解析 -
第22题:
单选题电离度和电离平衡常数都是表示弱电解质的相对强弱,它们之间的关系是()。A电离度越大,电离平衡常数越大;
B浓度越稀,电离度越大,电离平衡常数越大;
C在相同的温度下电离度可变,而电离平衡常数不变;
D多元弱酸的每一步电离平衡常数是相同的
正确答案: C解析: 暂无解析 -
第23题:
单选题某碱在18℃时的平衡常数为1.84×10-5,在25℃时的平衡常数为1.87×10-5,则说明该碱()。A在18℃时溶解度比25℃时小
B的电离是一个放热过程
C温度高时电离度变大
D温度低时溶液中的氢氧根离子浓度变大
正确答案: B解析: 暂无解析
